lunes, 27 de febrero de 2017
domingo, 26 de febrero de 2017
Por qué su pelo es liso o rizado: la ciencia lo explica
La razón por la que su pelo es liso o rizado no es algo sencillo, ni trivial. Por un lado, el tipo de formato capilar es tan potente como para amargar psicológicamente parte de la adolescencia y juventud de cualquier chaval, bien porque su imagen a lo afro le hace ser el diferente del grupo, por ejemplo, o porque su melena lacia es incompatible con lucir un peinado con gracia y volumen. Por otro lado, he aquí lo que nos interesa, detrás de un solo pelo se esconde un batallón de intrigantes circunstancias biológicas, genéticas y fisiológicas que explican por qué una fibra capilar puede ser curvada o recta.
A modo de curiosidad diremos que según los datos que difunde la empresa estadounidense de genómica nutricional GB HealthWatch, basados en las investigaciones de los doctores del Instituto de Investigación Médica de Queensland (Australia), el 45% de la población caucásica en Europa tiene el cabello liso, otro 40% lo luce ondulado, y un 15% pertenece al grupo de lo que popularmente se conoce como rizo cerrado. Por el momento, lo que la ciencia cuenta al respecto es que el hecho de pertenecer a una categoría u otra, de forma natural, depende de tres elementos interrelacionados.
“La predisposición genética y los factores internos que heredamos de nuestros antepasados son los que hacen que una persona nazca con el pelo liso o con el pelo rizado”, comenta la doctora Xenia Vorobieva, dermatóloga estética del Institut Vila-Rovira, especialistas en recuperación de pelo y estética capilar. En gran medida, como apunta la experta, son estos genes los que van a determinar casi todo. Concretamente, uno con nombre propio: TCHH. Es el que genera la proteína Tricohialina, presente en las células que conforman cada folículo y que, por tanto, tiene mucho que decir a la hora de dar resistencia y forma a la raíz del pelo. Porque el folículo también es clave, pero esto lo explicaremos más adelante. Con respecto al TCHH el gran descubrimiento llegó en 2009, cuando los mencionados científicos del Instituto de Investigación Médica de Queensland hallaron que una mutación de este gen era responsable de la formación del pelo rizado entre un porcentaje de la población europea. Su presencia en el ADN de cada persona marcaba la diferencia entre quienes tenían la cabellera lisa y los que la lucían rizada. LEER MÁS.
miércoles, 22 de febrero de 2017
¿Editaría los genes de su próximo hijo para que fuera mejor que el anterior?
''La genética podría permitirnos crear individuos más listos, bellos y longevos''.
El procedimiento de una prueba genética es muy sencillo: se toma una muestra de saliva y se envía al laboratorio donde se extrae ADN de las células.
Hay tests de este tipo para saber la compatibilidad genética con su pareja y evitan en lo posible la afección de dolencias a su futuro bebé; para chequear a los donantes de óvulos y semen; para conocer genéticamente a un embrión antes de su implantación en el útero y para, en fin, anticiparse a un destino genético que cada vez más iremos manipulando para disfrutar de una mayor calidad de vida.
Ciertamente, suena a manipular la genética con la que vinimos al mundo, pero ningún comité ético cuestiona el tratamiento de enfermedades específicas. “La mayoría de bioéticos distingue sabiamente entre la terapia génica aplicada a células somáticas (no sexuales) y a las reproductivas o germinales”, explica Blanca Laffon, profesora titular de Psicobiología en la Universidad de A Coruña y coautora del libro Terapia génica (CSIC y Catarata).
La terapia de células somáticas sigue los mismos principios que las terapias con fármacos habituales, pero los referentes a las células reproductoras son más difíciles de clarificar.
Hoy ya es posible librar a la descendencia de según qué enfermedades genéticas mediante la fecundación in vitro y la selección de embriones, y eso no implica demasiadas aclaraciones éticas. Pero ¿y si lo que se persiguiera es la mejora de la condición genética del individuo, incrementando su esperanza de vida, o su belleza, inteligencia o aptitudes deportivas?
Como casi todo en la vida, si se acaba haciendo un uso perjudicial de una tecnología tan sumamente prometedora, la culpa, desde luego, no será de la ciencia, sino de aquellos que, como en todos los campos, ven en los descubrimientos provechos que nada tienen que ver con el bien común. Será imprescindible blindar a nivel internacional a los comités de bioética del mundo para que, a modo de test genético, se anticipen a todos esos riesgos.
Pero las aplicaciones de conocer cuál es su material genético no se limita únicamente al posible diseño a medida de su descendencia. La ciencia camina hacia una futura medicina personalizada.
20 años de la oveja Dolly: ¿por qué los clones mueren jóvenes?
En 1997, los biólogos Keith Campell e Ian Wilmut presentaron al mundo a la oveja Dolly. Con ella nació una revolución científica y social
Fuente: elpais.com
lunes, 20 de febrero de 2017
Una terapia génica devuelve la audición a ratones sordos
La terapia génica trata de corregir errores genéticos que producen enfermedades. Para conseguirlo, una de las vías más frecuentes consiste en infectar al paciente con el gen adecuado empleando un virus. Las dificultades de la técnica hacen que, por el momento, se mantenga como un tratamiento principalmente experimental, que solo se emplea en pacientes que no tienen ninguna otra alternativa.
La revista Nature Biotechnology publica hoy dos resultados interesantes para el tratamiento de problemas del oído empleando este tipo de técnicas aunque, por ahora, los únicos beneficiados son ratones. Los dos trabajos van dirigidos a enfermedades auditivas de origen genético, un tipo de dolencias que afectan a alrededor de 125 millones de personas en todo el mundo.
Una de las principales dificultades a las que se habían enfrentado los científicos cuando trataban de llevar los genes correctos hasta la región del oído donde se encuentra el defecto es encontrar el vector adecuado. Hasta ahora, los virus empleados para el transporte no eran capaces de entrar en las células del oído interno que perciben las ondas sonoras.
En el primero de los dos artículos publicados en Nature Biotechnology, codirigido por Konstantina Stankovic, Jeffrey Holt y Luk Vandenberghe, todos miembros de instituciones asociadas a la Universidad de Harvard, en Boston (EEUU), los autores muestran cómo lograron introducir un gen que produce una proteína fluorescente en las células ciliadas internas y externas del oído de un ratón. Para conseguirlo, emplearon una variante sintética de un virus, Anc80L65, que infecta a los humanos sin hacerlos enfermar. Además de llevar los genes hasta su destino, el experimento mostró que la introducción de los genes no tiene efectos secundarios.
En un segundo artículo, otro grupo de la misma universidad liderado por Gwenaëlle Géléoc utilizó el mismo virus para tratar a ratones con síndrome de Usher. Esta enfermedad genética causa sordera, problemas de equilibrio y ceguera. Los investigadores introdujeron una copia normal del gen mutado, el Ush1c, en ratones con la enfermedad poco después de su nacimiento. El tratamiento hizo que se incrementasen los niveles de la proteína producida por ese gen cuando funciona correctamente y eso se tradujo en una recuperación de la audición.
En primer lugar, los autores pusieron a prueba a los ratones que antes eran sordos sometiéndolos a ruidos fuertes para ver si se asustaban. Además de responder positivamente a esa prueba, los ratones fueron sometidos después a mediciones de las regiones auditivas de su cerebro. Así, observaron que 19 de 25 ratones percibían sonidos menos intensos, por debajo de los 80 decibelios, el equivalente a una oficina con más de diez personas. El grupo que más beneficio recibió del tratamiento llegó a percibir sonidos de hasta 25 decibelios, una sensibilidad normal para un ratón. Los autores comprobaron también que el tratamiento mejoró los problemas de equilibrio asociados al síndrome de Usher.
Para trasladar estos resultados a los humanos, aún queda un trayecto importante. Por un lado, los responsables del estudio mencionan la necesidad de realizar el tratamiento justo después del nacimiento. Cuando la terapia se retrasó más de diez días, no tuvo efecto. Ahora, quieren probar su técnica en animales más grandes y con otras formas de pérdida auditiva de origen genético. En total, hay más de 100 defectos genéticos que producen enfermedades de este tipo.
domingo, 19 de febrero de 2017
Científicos descubren los genes que nos dejan calvos
Hasta ahora, habíamos conseguido relacionar la alopecia con un grupo
pequeño de genes. Sin embargo, una investigación llevada a cabo por
científicos de la Universidad de Edimburgo (Escocia) ha descubierto un
total de 287 genes implicados en la posibilidad de desarrollar calvicie.
Se trata del estudio más amplio sobre la relación entre la pérdida de cabello y la genética.
Los investigadores examinaron los datos genéticos y de salud de 52.874
personas (hombres blancos británicos de entre 40 y 69 años), con una
edad media de 57,2 años. De todos ellos, 16.724 (el 31.6%) no tenían
pérdida de cabello, 12.135 (el 23.0%) sufrieron pérdida leve de cabello;
14.234 hombres (el 26.9%) sufrieron pérdida moderada de cabello y
finalmente 9.781 (el 18.5%) perdieron cabello de forma severa.
Consiguieron localizar finalmente hasta 287 regiones genéticas
involucradas en la estructura y desarrollo del pelo; la mayoría forman
parte de cromosomas no sexuales, pero ciertamente una parte sustancial
(13 genes) pertenece al cromosoma X, el que los varones heredan de las
madres.
Diseñaron
una fórmula que logró identificar a personas predispuestas a
desarrollar calvicie severa a partir de la presencia o ausencia de
ciertos marcadores genéticos en su ADN. Sin embargo, no se trata de
predicciones individualizadas, sino del establecimiento de subgrupos de
población en los que el peligro de perder el pelo es bastante más
elevado que en otros. Pese a las limitaciones del estudio (el no poder
hacer una predicción individualizada exacta), se trata de un gran avance
en la comprensión de la arquitectura genética de la calvicie de patrón
masculino.
jueves, 16 de febrero de 2017
CREAN LA PRIMERA HAMBURGUESA DE CÉLULAS MADRE DE VACA
La carne, que fue degustada en Londres por dos expertos culinarios, mantiene las mismas características biológicas que la producida por el animal de manera natural, aunque con una importante reducción de la grasa presente en el músculo. Tiene, por tanto, idéntica apariencia y textura, pero un sabor ligeramente distinto. Los investigadores insisten en que no es perjudicial para la salud y se puede consumir sin miedo, ya que procede del propio tejido de la vaca.
Este podría ser el primer paso hacia la producción en masa de comida in vitro respetuosa con el medio ambiente, y que además podría contribuir a paliar contra el hambre en el mundo.
lunes, 13 de febrero de 2017
Descubren una terapia celular contra la demencia
Los biólogos han conseguido imitar en el
laboratorio el proceso de aparición de un defecto genético que acaba
dando forma a un grupo de demencias frontotemporales y han conseguido
corregirlo.
Biólogos moleculares de la Universidad Católica de Lovaina, en Flandes, han encontrado un nuevo método con células madre
que podría facilitar el desarrollo de un tratamiento contra la demencia
frontotemporal, informaron los investigadores en la publicación Stem
Cell Reports.
La
demencia frontotemporal es el nombre de un grupo de demencias
progresivas que afectan principalmente a la personalidad, al
comportamiento y al habla de un individuo.
Philip Van Damme y
Catherine Verfaillie, planificadores del proyecto, se apoyaron en tres
pacientes con una mutación en el gen de la progranulina GNR para crear
líneas de células madre pluripotenciales inducidas.
Después
indujeron una diferenciación cortical y posteriormente permitieron que
los neuroprogenitores madurasen hacia neuronas corticales.
Los
investigadores descubrieron en su trabajo un defecto en la generación de
neuronas corticales relacionado con la mutación GRN y una "vía de
señalización" específica, denominada Wnt, que es importante para el
desarrollo neuronal.
Se detectó que ese elemento "impide a las
células convertirse en células maduras del córtex cerebral", dijo
Catherine Verfaillie al diario flamenco De Morgen.
El
equipo de investigadores ha determinado que se puede corregir ese
defecto a través de la manipulación genética o un tratamiento que inhibe
la vía de señalización Wnt para así restaurar la capacidad de las
células madre pluripotenciales inducidas de convertirse en neuronas
corticales.
"Este
es el primer paso hacia el desarrollo de un medicamento. La
investigación se centra ahora en moléculas específicas que actúan de una
manera específica. Esperamos llegar a ese punto de aquí a pocos años",
afirmaron desde la Universidad de Lovaina.
domingo, 12 de febrero de 2017
COMIENZAN LOS PRIMEROS TRASPLANTES DE RETINA CON CÉLULAS IPS EN HUMANOS
El Ministerio de Sanidad nipón ha aprobado los primeros ensayos clínicos para realizar trasplantes de retina en humanos empleando células de pluripotencia inducida (iPS) de donantes, un proceso que se aplicará a cinco pacientes durante la primera mitad de este año.
El procedimiento consiste en implantar en el receptor una nueva mácula elaborada a partir de iPS -un tipo de célula que se convierte en cualquier tipo de tejido mediante un proceso de reprogramación- donadas y almacenadas en bancos por la Universidad de Kioto, una de las cuatro instituciones participantes en el proyecto.
El Ministerio nipón de Sanidad lleva más de un año deliberando la aprobación de los ensayos, después de que la mujer objeto del primer trasplante en 2014 para tratar la degeneración macular, en este caso con sus propias células iPS, desarrollara una mutación.
Los investigadores se han centrado en estudiar el procedimiento con células de donantes porque consideran que es más económico y ahorra tiempo, a diferencia de la operación pionera de 2014.
En dicha operación se utilizaron células iPS de la propia paciente y por ello el coste total acabó alcanzando unos 100 millones de yenes. Para rebajar ese importe la Universidad de Kioto decidió ese mismo año crear un programa de biobancos de iPS elaboradas a partir de células sanguíneas de donantes de todo Japón.
Se cree que el uso directo de células de donantes abaratará el proceso al menos en un 80 por ciento. El profesor de la Universidad de Kioto Shinya Yamanaka es considerado el padre de las iPS -lo que le supuso en 2012 el Nobel de Medicina- por desarrollar el método para crear este tipo de células mediante la reprogramación de células ya maduras.
Células madre para tratar las heridas de la piel de mariposa
Estas instituciones son las encargadas de llevar a cabo un estudio clínico basado en la administración sistémica por inyección intravenosa de células madre mesenquimales alogénicas haploidénticas derivadas de médula ósea como tratamiento para una variante de la llamada enfermedad piel de mariposa, la epidermolisis bullosa distrófica recesiva.
El ensayo está actualmente en proceso de aprobación por parte de la Agencia Española de Medicamentos y Productos Sanitarios (Aemps). Aemps considera este diagnóstico de vital importancia ya que “permite conocer de forma inequívoca qué tipo de epidermólisis bullosa tiene el paciente”. Además, permite recibir asesoramiento genético de cara a una planificación familiar y poder participar en ensayos clínicos como el actual.
Trasplantes de células madre podrían remitir la esclerosis múltiple a largo plazo
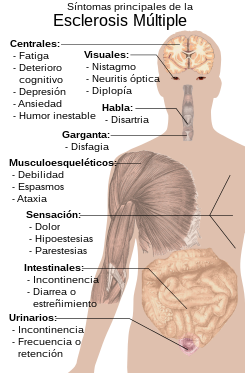 Los síntomas de la esclerosis múltiple varían ampliamente y pueden incluir dificultades motoras y del habla, debilidad, cansancio y dolor crónico. La forma remitente-recurrente es la más frecuente pero con los años se puede producir un empeoramiento y cambiar hasta una forma más progresiva de la enfermedad.
Los síntomas de la esclerosis múltiple varían ampliamente y pueden incluir dificultades motoras y del habla, debilidad, cansancio y dolor crónico. La forma remitente-recurrente es la más frecuente pero con los años se puede producir un empeoramiento y cambiar hasta una forma más progresiva de la enfermedad.
En el estudio los investigadores probaron la seguridad, eficacia y durabilidad del tratamiento en 24 pacientes de 26 a 52 años que, a pesar de tomar medicamentos clínicamente disponibles, experimentaron una inflamación activa, con frecuentes recaídas severas y un empeoramiento de su capacidad neurológica.
El tratamiento experimental pretende suprimir la enfermedad activa y prevenir una mayor discapacidad mediante la eliminación de las células causantes de enfermedades y el restablecimiento del sistema inmunológico. Durante el procedimiento, los médicos guardan las células madre sanguíneas del paciente para posteriormente someterles a dosis altas de quimioterapia hasta agotar su sistema inmune. Tras esto, vuelven a administrarles sus propias células madre para que reconstruyan el sistema inmune. Aunque uno de los riesgos que conlleva el tratamiento es que están más expuestos a infecciones cuando se encuentran inmunodeprimidos. De hecho, tres participantes fallecieron durante el estudio, aunque ninguno estuvo relacionado con el tratamiento.
Cinco años después del tratamiento, la mayoría de los participantes del ensayo permanecieron en remisión y la enfermedad se había estabilizado. Además, algunos participantes mostraron mejoras, como la recuperación de movilidad u otras capacidades físicas.
domingo, 5 de febrero de 2017
¿Tienen las plantas la facultad de ver?
Varias líneas de investigación recientes sugieren que las
plantas tienen la facultad de la visión y que hasta podrían poseer una
suerte de ojo, sumamente sencillo, eso sí.
La idea de que las plantas puedan tener
"ojos" no es nueva en absoluto. En 1907, Francis Darwin, hijo del
célebre Charles, planteó la hipótesis de que las hojas poseían unos
órganos, ahora llamados ocelos, que son una combinación de células
lenticulares y células fotosensibles. Los experimentos a inicios del
siglo XX confirmaron aparentemente la existencia de tales estructuras,
pero el concepto de "planta vidente" cayó en el olvido, hasta hace pocos
años, en que parece haber resurgido.
En uno de los últimos números de Trends
in Plant Science, František Baluška, experto en biología celular vegetal
de la Universidad de Bonn, y Stefano Mancuso, fisiólogo vegetal de la
Universidad de Florencia, exponen nuevos indicios sobre vegetales con
capacidad visual.
Para defender sus argumentos, los investigadores
señalan en primer lugar el descubrimiento en 2016 de que las
cianobacterias Synechocystis, microorganismos unicelulares que realizan
la fotosíntesis, actúan a modo de ocelos. "Estas cianobacterias se
sirven de la célula entera como lente para enfocar una imagen de la
fuente luminosa en la membrana celular, como si se tratara de la retina
del ojo animal", explica Conrad Mullineaux.
Induce a pensar en que
algo similar pueda existir en las plantas superiores.
Según trabajos recientes, ciertas
plantas como la col y Arabidopsis, pariente de la mostaza, fabrican
proteínas implicadas en el desarrollo y el funcionamiento de los ocelos,
los rudimentarios ojos de las algas verdes. Estas proteínas se
concentran en los plastoglóbulos, estructuras conocidas por otorgar a
las hojas otoñales sus tonos ocres y rojizos.
Si bien los indicios de estructuras
pseudooculares en las plantas superiores son escasos, no cesan de
surgir. "Jamás había oído hablar de la visión vegetal y no hubiera
creído en ella de no ser por mi descubrimiento de que las cianobacterias
operan como el ocular de una cámara", confiesa el biotecnólogo Nils
Schuergers, uno de los artífices del estudio de 2016 sobre
Synechocystis. El próximo paso será confirmar los experimentos que hace
más de un siglo revelaron que las propias células vegetales pueden
actuar a modo de lentes, y aún habrá que averiguar a qué fines sirve la
visión rudimentaria de las plantas.
Signos de rejuvenecimiento celular en la reprogramación ‘in vivo’
Un estudio del Centro Nacional de Investigaciones Oncológicas (CNIO) ha demostrado que durante el proceso de reprogramación in vivo, los telómeros de las células se alargan debido a un aumento de la telomerasa endógena. El trabajo se ha publicado en la revista Stem Cell Reports.
Las observaciones del equipo muestran que la reprogramación en tejidos vivos induce cambios característicos del rejuvenecimiento celular.
“Hemos comprobado que en un organismo adulto, cuando induces la desdiferenciación de las células, los telómeros se alargan, algo consistente con el rejuvenecimiento celular”, explica Maria A. Blasco, líder del Grupo de Telómeros y Telomerasa del CNIO y responsable del trabajo. Este alargamiento de los telómeros es un signo inequívoco de rejuvenecimiento celular, que se ha cuantificado por primera vez aquí en un organismo vivo.
Blasco y sus colegas han trabajado con los llamados “ratones reprogramables” –ideados por el también investigador del CNIO, Manuel Serrano, cuyo grupo también participa en este trabajo–. A grandes rasgos, las células de estos animales transgénicos portan los cuatro factores de Yamanaka (OSKM) que se activan con la administración de un antibiótico. Al hacerlo, las células retornan a un estadio similar al embrionario conocido como pluripotencia.
En virtud de la importancia de los telómeros en la regeneración de los tejidos, el envejecimiento y el cáncer, las autoras decidieron analizar los cambios que se producen en estas estructuras protectoras de los cromosomas durante el proceso de reprogramación in vivo, que lleva a la desdiferenciacion de los tejidos. Sus observaciones indican que este proceso conlleva un alargamiento de los telómeros, un marcador de rejuvenecimiento celular. Esta elongación se produce, según constata esta investigación, debido a la acción de la telomerasa. LEER MÁS.
Suscribirse a:
Comentarios (Atom)


